KEMIJA
Kemija je naravoslovna veda, ki preučuje snovi in osnovne spremembe. Snov je vse kar zavzema prostor in ima maso. Snovi so lahko naravne ali umetno pridobljene.

Sprememba agregatnega sranja:

Tri vrste sprememb:
- fizikalne spremembe (snov spremeni obliko)
- spremembe agregatnih stanj
- kemijske reakcije (snov nastane oz. se spremeni v drugo snov)
Mehanske lastnosti
Povedo nam, kako se material obnaša pri določenih obremenitvah. Med obremenitvijo lahko predmet spremeni svojo obliko, kemijska sestava pa ostane sepremenjena. (trda, mehka, krhka, elastična, toga…)
Električna prevodnost
Snov prevaja električni tok, če so v njej nabiti delci ali ioni, ki se lahko prosto gibljejo. Snov, ki prevaja električni tok je električni prevodnik. Kovine, taline in raztopine ionskih snovi. Snov, ki električnega toke ne prevaja je neprevodnik ali izolator.
Toplotna prevodnost
Kovine so dobri prevodniki toplote, najboljši Ag (srebro). Diamant je najboljši prevodnik toplote, vendar ne prevaja električnega toka. Slaba toplotna prevodnost - izolator.
Obstojnost
Predmeti, ki so narejeni iz različnih materialov so izpostavljeni raznim mehanskim in kemijskim vplivom. Življenska doba je odvisna od trajanja vplivov in intenszivnosti
Korozija je proces pri katerem razpada kovina.
Gostota snovi
Gostota snovi je odvisna od temperature - z višanjem temperature se gostota zmanjšuje. Na gostoto vpliva tudi tlak - z višanjem tlaka se viša gostota (to velja predvsem za pline). Trdne snovi imajo največjo gostoto, potem so tekočine in najmanjše gostote pa imajo plini.
Metode ločevanja zmesi in čiščenja snovi
Čiste snovi pridobimo s tem da jih ločimo od zmesi z uporabo metod ločevanja. Katero uporabimo je odvisno od snovi, ki zmess sestavljajo.
Sejanje
Odvisno od velikosti trdnih delcev, odvisno ali prihajajo skozi luknjice v situ. Uporablja se ga v kmetijstvu, industriji, gospodarstvu…
Dekantiranje / odlivanje
Odvisno od velikosti in topnosti delcev v topilu. Vsedanje večjih delcev na dno in odlivanje ali odtakanje zgornje tekočine.
Centrifugiranje
Je postopek ločevanja, pri kateremu s hitrim vrtenjem povzročimo, da se trdni delci, ki so v tekočini, zberejo na dnu posode. V centrifugi se ločujejo naprimer krvne celice of plazme.
Sublimacija
Metoda uporabna predvsem za čiščenje snovi v laboratoriju. Ko želimo ločiti snov od ostalih snovi v zmesi. (Snovi, ki sublimirajo - Jod, kafra, naftalen…)
Filtracija
Odvisno od velikosti in topnosti trdnih delcev v topilu (če dekantiranje ni možno, ker so delci premajhni). Primer je filtriranje pitne vode.
Izhlapevanje / izparevanje
Primer je izparevanje vode iz raztopine soli. Pridobivanje soli v solinah.
Ločevanje z magnetom
Odvisno od magnetnih lastnosti ene od snovi v zmesi (železo in NaCl).
Destilacija
Za ločevanje tekočin z različnimi vrelišči v snovi. Ločevanje glicerola in vode, frakcionirana destilacija nafte.
Ločevanje z lijem ločnikom
Za ločevanje tekočin, ki se ne mešajo. Uporabna predvsem za čiščenje snovi v laboratoriju.
Osnove toksikologije
Toksikologija je veda o strupenih snoveh in njihovem učinkovanju.
“Ni strupene snovi. Le odmerek ločuje strup od zdravila” - Parcelsius
Nevarne snovi lahko v telo vstopijo na več načinov:
- oralno (z zaužitjem)
- dermalno (skozi površino kože)
- inhalatorno / respiratorno (z vdihovanjem)
- intravenozno (vbrizgavanje v žilo)
- subkutalno (v podkožje)
Učinek škodljive snovi je odvisen od številnih dejavnikov:
- strupenosti
- količine v organizmu
- časa po izpostavitvi
- koncentracije
- načina vstopa v organizem
- mase človeka
- zdravstvenega stanja
TVEGANJE = NEVARNOST x IZPOSTAVLJENOST
Nevarnost = strupenost lastnosti snovi
Izpostavljenost = količina časa in pogostost kontakta / izpostavljenosti
Izpostavljenost
- količina snovi (odmerek / doza)
- meri se v mg/kg telesne mase
- nestrupenih snovi ni
- navadno velja da večja kot je količina, bolj je škodljiva
- čas in pogostost
- učinek je lahko različen po enkratni ali ponavljajoči izpostavljenosti
AKUTNA STRUPENOST - enkraten odmerek
KRONIČNA STRUPENOST - večkratni oz. ponavljajoči odmerek
Pogosto so znaki enkratne izpostavljenosti povsem drugačni od kronične.
| alkohol | učinki |
|---|---|
| 1 kratni | slabost, bruhanje, motnje ravnotežja… |
| večkratni | zasvojenost, nespečnost, citoza jetr… |
Strupi
Povzročijo smrt ob zaužitju snovi.
Odnos med učinkom in odmerkom
Kadar so toksični učinki odvisni od odmerka lahko za akutno toksičnost določimo LD50.
LD50 (lethal dose) je odmerek (mg snovi / kg mase telesa) ki povzroči smrt pri 50% izpostavljenih organizmov (živali). Običajno se navaja še način vnosa in vrsto ???
Označevanje nevarnih snovi
Znak za nevarnost (piktogram).
H (hazard) in P (precautionary) stavki.
Stavki o nevarnosti
- H (hazard) stavki o nevarnostih, opozorila na nevarnosti, izjave o nevarnostih. Opišejo nam učinek kemikalij na organizem / opremo.
- P (precautionary) stavki o previdnostnih ukrepih (obvestila…). Opišejo nam kje in kako snovi hranimo, kako ravnamo ob uporabi, kako ukrepamo pri poškodbah.
Zgradba atoma

Jedro je iz protonov in nevtronov. Elektronska ovojnica je iz elektronov.
| Delec | Simbol | Masa | Relativni naboj |
|---|---|---|---|
| proton | \(p^+\) | 1,6726 x 10-24g | +1 |
| nevtron | \(n^0\) | 1,6749 x 10p-24g | 0 |
| elektron | \(e^-\) | 0,00091094 x 10p-24g | -1 |
Element v periodnem sistemu:

79 je vrstno število. Au je simbol in 196.967 je relativna atomska masa.
Vrstno ali atomsko število = število protonov / elektronov. Masno število = št. protonov + nevtronov (zaokrožena relativna masa). Masno število tudi pove koliko \(n^0\) in \(p^+\) ima ta element v svoji v naravi najbolj razširjeni različici.
Torej element Au (zlato) z vrstnim številom 79 ima 79 elektronov in 79 protonov. Število nevtronov dobimo tako, da zaokroženemu masnemu številu (iz 196.967 zaokrožimo na 197) odštejemo vrstno število. Torej 197 - 79 = 118 nevtronov.
Izotopi
So atomi istega elementa, ki ise razlikujejo v številu \(n^0\).
Izotopi vodika:

Izotopi istega elementa imajo:
- različna masna števila
- različne fizikalne lastnosti
- različno razširjenost v naravi
- enako št. \(p^+\) in \(e^-\)
- enake kemijske lastnosti
- elementi imajo lahko en naraven izotop: \(^9\mathrm{Be}\), \(^{19}\mathrm{F}\), \(^{23}\mathrm{Na}\)
- lahko imajo tudi več naravnih izotopov: \(^{18}\mathrm{O}\), \(^{17}\mathrm{O}\), \(^{8}\mathrm{O}\)
Umetno pridobljeni izotopi nastanejo pri jedrskih reakcijah predvidoma so radioaktivni izotopi. Od vseh jedrskih reakcij je najpomembnejša radioaktivnost. Po je spontan razpad nestabilnh jeder na bolj stabilne delce / produkte.
Jedrska energija
Izotopi Urana U

| Izotop Urana | Razširjenost v naravi |
|---|---|
| 234U | > 0,0005% |
| 235U | 0,72% |
| 238U | 99,275% |
Uran U, ki ga danes uporabljamo kot jedrsko gorivo je po pridobitvi iz rude potrebno prečistiti in obogatiti. Jedrsko gorivo vsebuje 5% 235U in 95% 238U. Za to uporabljajo razlike v fizikalnih lastnostih. V gorivnih palicah iz urana je jedrsko gorivo v obliki UO2. Skupaj ∼ 50 ton urana.
Nadzorovana jedrska reakcija

Nenadzorovana pa bi bila / je atomska bomba.
Jedrska energija → uparevanje vode → turbine → el. generatorji.
Element ali prvina
To je snov, ki je ne moremo razgraditi v enostavnejše delce / snovi. Izgrajen je iz ene same vrste atomov.
Simboli elementov
Enočrkovni ali dvočrkovni simboli. Izvor imen: po zemljepisnih imenih, bogovih, mitoloških bitjih, planetih, znanstvanikih, nebesnih telesih…
Periodni sistem
Začetek 19.stoletje → 35 elementov
Konec 19.stoletje → 70 elementov
Danes → 118 elementov (92 v naravi, ostali pa umetno pridobljeni)
V periodnem sistem so uvrščeni po vrstnem številu.
| I | II | III | IV | V | VI | VII | VIII |
|---|---|---|---|---|---|---|---|
| 1 | 2 | 13 | 14 | 15 | 16 | 17 | 18 |
7 period:
| Perioda | Elementi |
|---|---|
| 1 | Alkalijske kovine |
| 2 | Zemeljsko alkalijske kovine |
| 3 - 6 | prehodne kovine |
| 7 | Halogeni elementi |
| 8 | Žlahtni plini |
| ostalo | Lantanoidi + aktinoidi |
Na levi strani so večinoma kovine, na desni pa polkovine in nekovine. Elementi, ki se nahajajo v obliki dvoatomne molekule: N2, O2, H2, O3, F2, Cl2, Br2, I2.
Simbol elementa O ≠ formula elementa (O2)
Elementi, ki so pri sobni temperaturi plini:
H2, O2, N2, F2, Cl2, žlahtni plini.
Elementi, ki so pri sobni temperaturi tekoči:
Hg, Br2.
Kovine
- Vse kovine razen Hg so v trdnem agregatnem stanju.
- Imajo kovinski sijaj.
- Prevajajo električni tok in so dober prevodnik toplote.
- Lahko jih kujemo in vlečemo.
- Večinoma tvorijo trdne kristale.
- V ionskih spojinah jih najdemo v obliki kationov (+).
Alkalijske kovine
- Mehke in najbolj reaktivne kovine.
- V naravi jih najdemo le vezane v spojine.
- Z vodo burno reagirajo.
- Litij, Natrij
- Kalij so tako reaktivni, da ne smejo priti v stik z zrakom, zato jih moramo hraniti v petroleju, Rubidij in Cezij pa v zataljenih ampulah.
Aluminij (Al)
- Mehka, srebrno bela, polsvetleča kovina.
- Majhna gostota 2,7g/cm3 (lahka kovina).
- Odporen na atmosferske vplive (dolga življenska doba).
- Odlična električna prevodnost (edini material, ki je primeren za prevod električnih energij visoke napetosti).
- Dobra sposobnost oblikovanja in preoblikovanja.
- Kovina z največjo toplotno prevodnostjo (radiatorji).
- Omogoča ponovno uporabo (reciklaža).
- Prodobljena je iz rude Baksit.
Zlato (Au)
- Mehka svetleče rumena kovina.
- Je najbolj kovna kovina.
- Na zraku ne oksidira - uporabna za električne kontakte.
- Nakit - Au dodajajo druge kovine, da povišajo trdoto.
Baker (Cu)
- Svetlordeča, žilava in mehka kovina.
- Pridobiva se iz bakrove rude - halkopirit+.
- Dober električni prevodnik - električni vodniki, telefonske žice.
- V vodi ni podvržen koroziji - vodovodne cevi.
- Na zraku oksidira - obda se z patino (stabilni oksid), ki preprečuje nadaljno korozijo.
Železo (Fe)
- Trda, močna in žilava kovina.
- Najpogostejša kovina v zemeljski skorji.
- Cenena in zatonajbolj uporabljena kovina v industriji in gradbeništvu.
- Pridobivajo jo iz železovih rud, ki vsebujejo minerale, kot so hematit in magnetit.
- Na zraku hitro korozira (rjavenje).
Titan (Ti)
- Trdna in lahka kovina, ki je zelo odporna na korozijo.
- Uporabna v letalski industriji, urarski industriji in medicini (umetni kolki in kolena).
Zlitine ali legure
Zlitina je homogena zmes dveh ali več kovin. Dobimo jih z mešanjem raztaljenih kovin, nastalo zmes pa pustimo, da se ohladi in strdi. Zlitine imajo lahko lastnosti od kovin iz katerih so narejene ali pa čisto posebne lastnosti.
Jeklo
- Zlitina železa, ogljika in drugih kovin.
- Večja trdota od železa.
- Nerjaveče jeklo - vsebuje še nikelj in krom.
Bron
- Zlitina bakra in kositra, včasih ima še cink, arzen ali kako drugo kovino (trši od železa).
Cin
- Zlitina bakra, svinca in kositra.
- Ima nizko tališče (uporabno za spajkanje).
Amalgam
- Zlitina živega srebra in drugih kovin (Ag, Sn, Cu, Zn).
- Uporablja se za rekonstrukcijo poškodb zob (plombe).
Polkovine
Imajo nekatere lastnosi kovin in nekatere lastnosti nekovin. Vse so v trdnem agregatnem stanju. So polprevodniki (pri določenih pogojih prevajajo električni tok).
Silicij
- Svetleč, krhek, prevaja el. tok. Slabo prevaja toploto.
- Uporaben v elektronskih vezjih.
Nekovine
Ne prevajajo električnega toka (razen grafita) in slabo prevajajo toploto. Najdemo jih v vseh treh agregatnih stanjih. Ne moremo jih kovati in vleči. V ionskih spojinah jih najdemo v obliki negativnih ionov (anionov).
Vodik (H)
- \(\mathrm{H_2}\) je najlažji plin (14,4 x lažji od zraka) in zelo reaktiven.
- V mešanici s kisikom (\(\mathrm{O_2}\)) je eksploziven.
- Nastaja pri raztapljanju nežlahtnih kovin v kislinah.
\( \phantom{plac} \mathrm{ Mg_{(s)} + 2HCl_{(aq)} \rightarrow MgCl_{2\phantom{a}(aq)} + H_{2\phantom{a}(g)} } \)
- H2 je ekološko gorivo prihodnosti (gorivne celice).
Kisik (O)
- O2 je plin brez barve, vonja in okusa.
- V atmosferi ga je približno 21%.
- Topen je v vodi (topnost pada s temperaturo).
- Pospešuje gorenje, sam pa ne gori.
- Kemijsko je zelo reaktiven in tvori spojine (oksidi skoraj z vsemi elementi periodnega sistema razen z žlahtnimi plini).
- Gostejši od zraka, živim bitjem nujno potreben za dihanje.
Dušik (N)
- Pri sobni temperaturi nereaktiven plin.
- Pridobivajo ga s frakcionalno destilacijo utekočinjenega zraka.
- Največ dušika se porabi za proizvajanje amonijaka (umetno gnojilo).
- Zradi nizkega vrelišča je izjemno učinkovito hladilno sredstvo.
- Tekoči dušik (-196oC), se uporablja za shranjevanje bioloških in medicinskih preparatov v industriji za hlajenje.
Halogeni elementi




Fluor (F)
- Najbolj reaktiven element - reagira skoraj z vsemi elementi.
- Najmočnejši oksidant od vseh elementov v periodnem sistemu.
- V naravi se nahaja vezan v spojinah (npr CaF2).
- Uporaba: njegove spijine najdemo v zobni pasti (preprečevanje kariesa).
- Fluorovodikova kislina HF - za jedkanje stekla.
- Pri pripravi polimera teflona (PTFE).
Klor (Cl)
- Strupen rumenozelen plin zadušljivega vonja, ki se topi v vodi.
- Uporaba: za razkuževanje vode, bojni strup, izdelava polimerov (pvc), priprava insekticidov (DDT)…
Brom (Br)
- Uporabljen pri izdelavi fotografskih filmov.
- Za pripravo obrambnega plina (tear gas).
- Za izdelavo zatiralcev požara.
Jod (I)
- SIva trdna snov.
- Pri visoki temperaturi sublimira, jodove pare so vijolične barve.
- V vodi se skoraj ne topi, se pa v etanolu.
- Raztopini Joda v etanolu rečemo jodova tinktura.
- Jodovica pa je raztopina joda in kalijevega jodida.
- Uporaba: tinktura v medicini za razkuževanje. Spojine joda dodajamo prehrani, pomanjkanje joda v prehrani povzroča golšavost. Pri izdelavi zdravil za rakava obolenja. Jodovico se uporablja za dokazovanje škroba v živilih.
Žlahtni plini
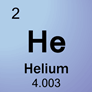




So zelo stabilni in nereaktivni plini.
Zrak in plini
| Plin | delež v ozračju |
|---|---|
| \(\mathrm{ N_2 }\) | ≃ 78% |
| \(\mathrm{ O_2 }\) | ≃ 21% |
| \(\mathrm{ CO_2 }\) + ostali | ostalo |
Plini
| Ime in formula | Uporaba |
|---|---|
| \(\mathrm{ He }\) - helij | baloni |
| \(\mathrm{ N_2 }\) - dušik | hlajenje, zmrzovanje |
| \(\mathrm{ CO_2 }\) - ogljikov dioksid | gasilno sredstvo, gaziranje pijač |
| \(\mathrm{ NH_3 }\) - amonijak | gnojilo |
| \(\mathrm{ CH_3 }\) - metan | gorivo |
| \(\mathrm{ N_2O }\) - došikov dioksid | smejalni plin “anestetik” |
| \(\mathrm{ Cl_2 }\) - klor | razkižilo, belilo |
Lastnosti plinov
- Nimajo stalne oblike in prostornine
- Delci v plinu se prosto gibljejo
- Plini se med seboj mešajo
- Imajo majhno gostoto
Ogljikov dioksid (CO2)
- \(\mathrm{CO_2}\) je brezbarven negorljiv plin.
- Nastaja pri postopku gorenja organskih snovi.
- Nastaja pri celičnem dihanju številnih mikroorganizmov, proizvajajo ga pri fermentaciji.
- Večja gostota od zraka, zato se zadržuje pri tleh.
- Rastline ga uporabljajo pri fotosintezi.
- Se zelo dobro topi v vodi in povzroča kislost vode, zato voda raztopi apnenec.
- Uporablja se za izdelavo gaziranih pijač.
- \(\mathrm{CO_2}\) se uporablja pri varjenju kot zaščitni plin, saj je v primerjavi z Ar veliko cenejši.
- \(\mathrm{CO_2}\) je suhi led (hlajenje).
- Uporablja se ga kot sredstvo za gašenje.
Pojav tople grede
- Dogaja se zaradi prevelike količine \(\mathrm{CO_2}\) in ostalih toplogrednih plinov.
Izvor toplogrednih plinov
- Sežig fosilnih goriv (premog, nafta, plin…)
- Krčenje gozdov, industrija, promet.
- Uporaba umetnih gnojil v kmetijstvu.
Toplogredni plini
- Vodna para
- \(\mathrm{CO_2, O_3}\)
- Metan \(\mathrm{CH_3}\)
- Klorofluorovodiki \(\mathrm{CFC}\)
- Didušikov oksid \(\mathrm{N_2O}\)
Del sončne energije se odbije od oblakov ozračja in zasneženih površin zemlje. Odbito IR svetlobo absorbirajo molekule toplogrednih plinov in jo nato oddajo v okolico in sicer v vse smeri, polovico nazaj na zemljo.

Večji del dončne svetlove absorbira površje in jo segreva. Segreta površina zemlje seva IR svetlobo.
Posledice globalnega segrevanja
- Spremenjene vremenske razmere.
- Povečana temperatura ozračja.
- Taljenje ledu in ledenikov.
- Dvig morske gladine.
Reševanje problema
- Zamenjava fosilnih goriv z drugimi energetskimi viri ter varčna / učinkovitejša izraba energije / zmanjševanje energetskih potreb.
- Skladiščenje CO2 in pretvorbo v metan (biogorivo).
- Zajem CO2 in stisnjega CO3 po cevovodih.
- Skladiščenje (opuščeni rudniki, vrtnine, dno morja).
Obnovljivi viri energije
- Zaradi gospodarske rasti se višajo energetske potrebe.
- Potreba po energetskih virih ki manj škodijo okolju / ga ne uničujejo.
- Potreba po cenovno dostopni energiji.
Sončna energija
- Solarni sistemi za ogrevanje in osvetljevanje prostorov, fotovoltaika - sončne celice za proizvajanje sončne energije.
- Problem - visoka cena, nihanje v količini sončne energije ki pade na celice (letni čas, vreme…)
Vodna energija
- Najpomembnejši vir energije (21% vse električne energije na svetu)
- dolga življenska doba, nizki stroški obratovanja, visoki izkoristki
- velik poseg v okolje, visoka cena naložbe, nihanje glede na pretok (vreme, letni čas)
Biomasa
- velik izkoristek, izraba odpadnega materiala
- visoka cena investicije, negospodarno ravnanje z gozdovi
Geotermalna energija
- dolga življenska doba, nizki stroški obratovanja
- visoka cena investicije (vrtina), posedanje tal, onesnaženje s paro in plini (H2S, CO2, NH3 …)
2858 words